 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
“玻璃构造”是指离子或原子在空间的几何配置以及它们在玻璃中形成的构造形成体。最有影响的近代玻璃构造的假说有:凝胶学说、无规章网络学说、晶子学说、五角形对称学说、高分子学说等,其中能够最好地解释玻璃性质的是()和无规章网络学说。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 答案
答案
 更多““玻璃构造”是指离子或原子在空间的几何配置以及它们在玻璃中形成的构造形成体。最有影响的近代玻璃构造的假说有:凝胶学说、无规章网络学说、晶子学说、五角形对称学说、高分子学说等,其中能够最好地解释玻璃性质…”相关的问题
更多““玻璃构造”是指离子或原子在空间的几何配置以及它们在玻璃中形成的构造形成体。最有影响的近代玻璃构造的假说有:凝胶学说、无规章网络学说、晶子学说、五角形对称学说、高分子学说等,其中能够最好地解释玻璃性质…”相关的问题
第1题
A.分子中原子之间的连接顺序与方式
B.原子或基团绕单键旋转所形成的不同空间形式
C.构造相同,原子或基团在空间的排列方式有差别
D.分子在不同溶剂中的存在形式
第2题
根据下列配离子的磁矩实验值,应用价键理论讨论配离子的形成过程及空间几何构型.
(1)[Mn(NCS)6]4-6.1BM
(2)[Co(NO2)6]4-1.8BM
(3)[Ni(NH3)4]2+3.2BM
(4)[CuCl4]2-2.0BM
第3题
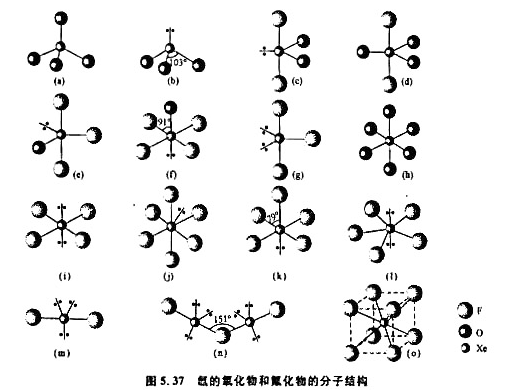
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?
第4题
A.NH3能做配位体,是由于氮原子具有孤对电子。
B.乙二胺中有两个原子提供孤对电子,故可以和中心离子形成两个配位键,所以乙二胺是双齿配体。
C.在中心离子中,必须具有孤对电子,以形成配位键。
D.配离子和配位分子统称为配位化合物。
第5题
A . 晶面
B . 晶粒
C . 晶格
D . 晶架
第10题
若BCl3分子中B原子采用sp2杂化轨道成键,则BCl3的空间几何构型是()。
A.平面三角形
B.直线形
C.四面体形
D.平面正方形
第11题
试用价层电子对互斥理论判断下列分子或离子的空间构型:

要求写出中心原子提供的价层电子数、配体提供的电子数、离子提供的电子数、价层电子总数、价层电子对数、电子对构型和分子(离子)构型。