 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g), e知在540~727 K之间发生定容反应,其速率常数k的表达
有双分子反应CO(g)+NO2(g)→CO2(g)+NO(g), e知在540~727 K之间发生定容反应,其速率常数k的表达式为
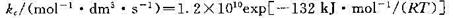
若在600 K时,CO(g )和NO2(g)的初始压力分别为667 Pa和933 Pa.试计算:(1)该反应在600 K时的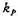 值;(2)反应进行10h后,NO的分压。
值;(2)反应进行10h后,NO的分压。
 答案
答案





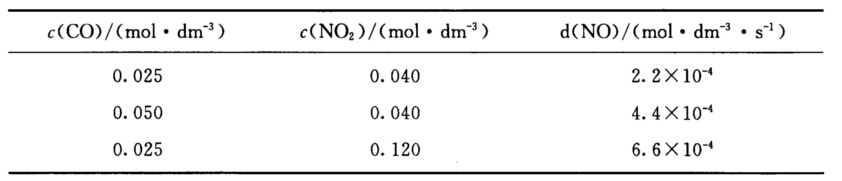 (1)写出反应的速率方程; (2)求650 K时的速率常数; (3)当c(CO)=0.10 mol.dm-3,c(NO2)=0.16 mol.dm-3时,求650 K时的反应速率; (4)若800 K时速率常数为23.0 dm3mol-1.s-1,求反应的活化能。
(1)写出反应的速率方程; (2)求650 K时的速率常数; (3)当c(CO)=0.10 mol.dm-3,c(NO2)=0.16 mol.dm-3时,求650 K时的反应速率; (4)若800 K时速率常数为23.0 dm3mol-1.s-1,求反应的活化能。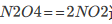 达平衡时总压为100kPa,N2O4有20%分解为NO2,则反应的K值为( )。
达平衡时总压为100kPa,N2O4有20%分解为NO2,则反应的K值为( )。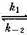 2NO2(g)的速率常数
2NO2(g)的速率常数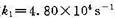 ,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为
,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为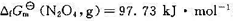 和
和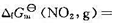 51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
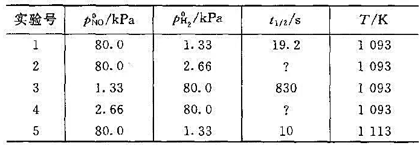
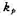 ;(3)求反应的活化能
;(3)求反应的活化能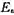 ;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,
;(4)提出一个只涉及双分子步骤的反应机理,由此机理可得上述规律;(5)如果1093K时,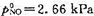 ,
,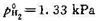 ,求该反应的半衰期。
,求该反应的半衰期。



















