题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
CH4分子中C原子是采取( )杂化轨道成键的
CH4分子中C原子是采取()杂化轨道成键的
A.sp
B.sp2
C.sp3
D.d2sp4
 答案
答案
查看答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.sp
B.sp2
C.sp3
D.d2sp4
 答案
答案
 更多“CH4分子中C原子是采取( )杂化轨道成键的”相关的问题
更多“CH4分子中C原子是采取( )杂化轨道成键的”相关的问题
第1题
A.凡中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体
B.CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合而成的
C.sp3杂化轨道是由同原子中能量相近的s轨道和p轨道混合起来形成的一组能量相等的新轨道
D.凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键
第2题
若BCl3分子中B原子采用sp2杂化轨道成键,则BCl3的空间几何构型是()。
A.平面三角形
B.直线形
C.四面体形
D.平面正方形
第3题
A.电子在整个分子范围内运动,不再属于某一特定原子
B.反键分子轨道的能量比所有成键分子轨道高,此当反键分子轨道上有电子时,分子不稳定
C.分子轨道是不同原子的原子轨道线性组合面成,杂化轨道是同一原子的原子轨道组合而成
D.只有符合对称性匹配、能量相近和最大重叠原则的原子轨道才能有效地组合成分子轨道
第7题
A、H2O
B、CH4
C、NF3
D、BF3
第10题
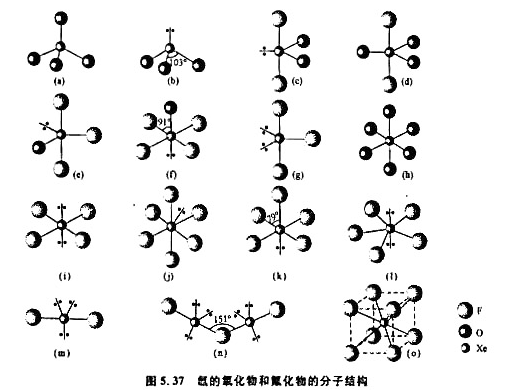
图5.37示出氙的氟化物和氧化物的分子(或离子)结构。
(1)根据图形及VSEPR理论,指出分子的几何构型名称和所属点群;
(2)Xe原子所用的杂化轨道;
(3)Xe原子的表观氧化态;
(4)已知在XeF2,XeF4,加合物晶体中,两种分子的构型与单独存在时的几何构型相同,不会相互化合成XeF2,从中说明什么问题?