 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
问题1、向含铜粉的稀硫酸中滴加浓硝酸,写出该反应的离子方程式()。问题2、制备流程中的A操作名称是()。如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4•5H2O中可能存在的杂质是(),除去这种杂质的实验操作称为()问题3、如果采用重量法测定CuSO4-5HO的含量,完成下列步骤。①()②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略)。在过滤前,需要检验是否沉淀完全,其操作是()。如果1.040g提纯后的试样中含CuSO•5HO的准确值为1.015g,而实验测定结果是1.000g,测定的相对误差为()问题4、已知:CuSO4+2NaOH→Cu(OH)2↓:1+Na2SO4.称取0.1000g某CuSO4•5H2O试样(杂质不与氢氧化钠溶液反应)于锥形瓶中,加入0.1000mo1/L氢氧化钠溶清28.00mL反府完全后,过量的氢氧化钠用0.1000mo1/L盐酸滴定至格点,托用盐酸20.16mL则0.1000g该试样中含CuSO4•5H2O()g上述滴定中,滴定管在用蒸馏水洗净之后,注入盐酸之前,还需进行的操作是()在滴定中,准确读数应该是滴定管上蓝线()所对应的刻度。
 答案
答案





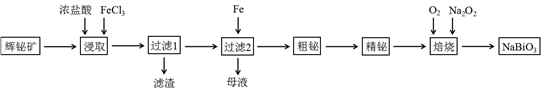 已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。
已知:①铋酸钠是一种难溶于水的物质;②水解能力:Bi3+>Fe3+。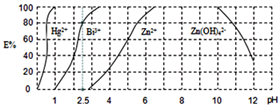 ①当n(Bi3+):n[Bi(HDz)3]=1:4时,废水的pH=()。
①当n(Bi3+):n[Bi(HDz)3]=1:4时,废水的pH=()。



















