 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
排盐苛化的机理是()。
A. 排除系统中多余的Na2CO3
B. Na2CO3的溶解度随NaOH浓度的升高而降低
C. Na2CO3的溶解度随温度的升高而升高
D. 排除系统中多余的腐植酸。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A. 排除系统中多余的Na2CO3
B. Na2CO3的溶解度随NaOH浓度的升高而降低
C. Na2CO3的溶解度随温度的升高而升高
D. 排除系统中多余的腐植酸。
 答案
答案
 更多“ 排盐苛化的机理是()。”相关的问题
更多“ 排盐苛化的机理是()。”相关的问题
第2题
第5题
应设有导除静电的接地装置。
A.排除、输送有燃烧或爆炸危险的粉尘的排风系统
B.排除、输送有燃烧或爆炸危险的气体的排风系统
C.排除、输送有燃烧或爆炸危险的蒸汽的排风系统
D.上述三项
第6题
A.密闭一通风排毒系统
B.开放式作业
C.局部排气罩
第9题
A.改革工艺,搞好清洁生产,减少“三废产生”
B.综合利用,变废为宝,进行资源化利用
C.消除污染、进行无害化处理,造福子孙后代
D.数量少可以直排,数量多稀释完了排放
第11题
简要回答下列问题:
(1)电解NaCl熔盐制取金属Na的过程中,为什么要加入CaCl2?由此带来的负面影响是什么?
(2)为什么金属Mg与冷水反应极慢,却可以迅速与热水或NH4Cl水溶液发生反应?
(3)什么是离子势φ?为什么φ的大小可以影响一些氧化物的水化物的解离方式?
(4)为什么加热MgCl2·6H2O时得不到无水盐?
(5)为降低煤炭燃烧时排向大气的SO2量,可以把CaO或CaCO3掺到含硫的煤炭中。试说明这种做法的化学原理,写出相关的化学反应方程式。
(6)Li+和Mg2+半径十分接近,试分析它们的碳酸盐分解温度的高低。
(7)锂的第一电离能比钠大,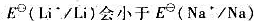 ?既然
?既然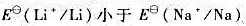 ,为什么锂与水的反应却不如钠剧烈?
,为什么锂与水的反应却不如钠剧烈?
(8)试说明锂的哪些性质与镁相似而有别于钠、钾。
(9)试说明铍的哪些性质与铝相似而有别于镁、钙。
(10)试用价层电子对互斥理论和杂化轨道理论,讨论XeF6分子的几何构型和中心原子的轨道杂化方式。